附: 胚胎移植术
一、胚胎移植的发展概况
胚胎移植也称受精卵移植,或者简称卵移植。它的含意是将一头良种母牛配种后早期胚胎取出,移植到另一头同种的生理状态相同的母牛体内,使之继续发育成为新个体,所以通俗地叫人工受胎或借腹怀胎。提供移植的个体称为供体,接受胚胎的个体叫做受体。胚胎移植实际上是由产生胚胎的供体和养育胚胎的受体分工合作共同繁殖的后代。
(一)胚胎移植的发展简史
1890年,英国剑桥大学赫普将4细胞的安哥拉兔的早期胚胎移植到1只已交配过的比利时野兔的输卵管内,获得2只安哥拉小兔,首次获得胚胎移植成功。20世纪30年代以后,胚胎移植成为生物科学研究主攻方向之一。牛的胚胎移植于1951年获得成功,就胚胎移植技术的发展情况看,可分为三个阶段: 20世纪50年代以前为实验生物阶段; 20世纪50~70年代可称为家畜实验阶段; 20世纪70年代以后为实际应用阶段。在美国、法国、德国、加拿大、英国、澳大利亚、日本等很多国家都建立了胚胎移植的企业机构。1973年威尔穆特把在液氮保存6天的牛胚胎经解冻后移植,得到1头公犊。胚胎超低温冷冻保存解冻技术的突破,是胚胎移植技术的重大成就,也是该项技术发展中的一次飞跃。
在国际范围内,牛胚胎移植研究最多,成果也最多。如牛卵体外受精后移植成功,手术移植鲜胚成功率 (受体妊娠率) 可达80%以上; 非手术移植的成功率达50%~70%。就大数量平均而言,每次由1头供体采得的胚胎,经移植最后可获得2~4头犊牛,冷冻胚胎移植成功率为30%~60%。美国和欧洲一些国家已走向商品化。美国每年胚胎移植10万头以上,其中多数为肉牛。日本继美国、加拿大之后,牛胚胎移植进展较快,2000年美国向世界上20多个国家出口胚胎约15万枚。
随着胚胎移植研究的不断深入,涉及的内容更加广泛。如胚胎性别鉴定后再移植,卵细胞体外培养,成熟和受精以及胚胎分割,均已取得进展,这将大大提高胚胎移植的实用价值。
我国胚胎移植研究从20世纪70年代中期或后期开始。目前奶牛胚胎移植受胎率一般可达50%~60%,冻胚受胎率一般在30%~40%。河北、吉林、山东、陕西、河南已将奶牛胚胎移植给黄牛获得成功。河北、吉林等地用奶牛胚胎移植给黄牛的妊娠率可达50%左右。有些胚胎工程如胚胎分割后移植 (包括移植给奶牛和黄牛)、核移植、牛体外受精后移植都有获得成功的例子。
(二)胚胎移植的意义
1. 可以迅速提高牛的遗传素质 由于超数排卵技术的应用,使1头优秀的母牛一次排出许多倍于平常的卵子数,免除了其本身的妊娠期和负担,因而能留下许多倍的后代数。一般可以从1头优秀母牛身上一年获得40~50头后代,大大加速品质改良速度,扩大良种牛群。
2. 保种和便于国际的贸易 胚胎库就是基因库,可以使我国不少优良地方良种牛借胚胎冷冻长期保存,而且胚胎的国际贸易可省去活体运输的种种困难。
3. 使肉牛产双犊,提高生产率 由胚胎移植技术演化出来的“诱发双胎” 的方法,即向已配种的母畜 (排卵对侧子宫角) 移植1个胚胎,这种方法不但提高了供体母牛的繁殖力,同时也提高了受体牛的繁殖率 (受胎率和双胎率)。另外还可以向未配种的母畜移植两个胚胎。这样在母牛头数不增加的情况下,降低繁殖母牛的饲料费用,增加经济效益,并可满足人类对肉类的需求增长。
4. 克服不孕 优秀母牛易发生习惯性流产或难产,及由于其他原因不宜负担妊娠过程的情况下 (如年老体弱),也可用胚胎移植,使之正常繁殖后代。例如美国科罗拉多州大学报道,1头长期屡配不孕的母牛通过胚胎移植在15个月期间内获得30头犊牛。
5. 其他 目前国内外,已利用胚胎移植技术作为研究受精作用、胚胎学、细胞遗传学等基础理论的研究手段。
(三)供体、受体的选择和准备
1. 供体的选择和准备
(1) 供体母牛具有优良的遗传性,必须是经过各方面鉴定表现优秀性状的个体,具有较高的育种价值。
(2) 供体母牛必须是健康的,并要经过血检及检疫,证明布氏杆菌病、结核、副结核、蓝舌病、牛黏膜综合征、钩端螺旋体病、传染性鼻气管炎、流行性感冒等均为阴性。
(3) 供体母牛生殖器官功能应处在较高水平。对供体牛的生殖道,要进行彻底检查,如生殖器官有无粘连、卵巢囊肿、卵巢炎和子宫炎等疾病。
(4) 做好选定供体发情症状及发情规律的观察。在超排处理中,发情症状及发情规律是极为重要的。不正常的母牛就会影响给药时间,进而影响激素的作用,结果造成超数排卵失败。对供体母牛至少连续观察两个发情周期,如果还有环境和饲养管理条件的变化,更应长期观察。发情周期过长和发情征候不明显,以及持续发情的母牛不能作供体。
(5) 供体牛的膘情要适中,过肥或过瘦都会降低受精率。
(6) 供体牛不仅要求经济性能突出,繁殖性能也非常重要。过去的妊娠配种不超过两个情期,而且没有发生过难产。在繁殖上没有缺陷。
(7) 个体反应的敏感性。卵巢对激素的反应依动物的种类不同而有显著的差异。但就母牛对超排处理的反应,个体间差异也很大。因此,很希望预知母牛的反应,以便选择反应敏感的母牛作为供体。超排反应和功能代谢有关,因此,要测定谷草转氨酶和胆固醇水平,正常者,超排反应好。
(8) 母牛在产后6~9周不宜用超排处理。1头母牛在一个泌乳期内不宜做两次以上的超排处理。一些产奶量很高的优秀奶牛,其超排效果往往较差,因此要特别注意给予良好的饲养管理。
(9) 年龄: 初产牛及8岁以内的经产牛均可作供体,超过10岁,受精率下降。
2. 受体牛的选择
(1) 每头供体牛需准备数头受体牛,受体母牛一般选用最宜使用,价格低廉的青年牛,如经产牛作受体,不得超过10岁。
(2) 受体牛应具有良好的繁殖性能,无生殖器官粘连。异性双胎牛、子宫和卵巢病、卵巢囊肿等不能作受体。
(3) 在拥有大数量母牛的情况下,可以选择自然发情与供体发情时间相同的母牛,两者的发情时间最好相同或相近,前后不应超过1天。
(4) 受体牛要具有良好的健康状态,体型中上等。检疫和疫苗接种与供体牛相同。
(5) 受体牛要隔离饲养,与其他牛及其饲料和饮水要严格分开。
二、同期发情
胚胎移植的成功率在很大程度上取决于供体与受体的发情同期化。这是因为在发情周期内,母畜生殖道的生理特点变化很大。两者差异大,移植后不利胚胎成活,甚至完全失败。因此要严格控制,使其一致,最多前后差异不得超过1天。在使用新鲜胚胎的情况下,胚胎必须当天移植,同期化尤其重要。发情同期化有两种含义: 一是受体的发情同期化,即1个供体,在正常超排情况下可以收集到可用胚胎7~8个,为其准备受体也需7~8个,因此受体牛要同期化; 二是供体和受体的发情同期化,也就是使同期化的一群受体牛和供体牛再同期化。
(一)同期发情的机制
同期发情的机制是以人工合成的激素制剂,模拟牛体内激素对卵巢作用,而使母牛的卵泡发育和排卵同期化。实现同期化有两条途径: 一是延长一群牛的黄体作用而抑制卵泡生长发育,然后一起停药,使卵泡成熟并排卵; 二是中断黄体,然后一起使卵泡发育排卵。
延长黄体,抑制卵泡发育的药有孕酮、甲孕酮、炔诺酮、氟孕酮、甲基孕酮、18-甲基炔诺酮、16-次甲基甲地孕酮,以及氯地孕酮等。促进黄体退化的药物有前列腺素。促使卵泡发育排卵的有孕马血清促性腺激素 (PMSG)、人绒毛膜促性腺激素 (HCG)、促卵泡素 (FSH)、促黄体素 (LH)、促黄体素释放激素 (LHRH) (即促性腺激素释放激素)。
(二)牛的同期发情方法
1. 前列腺素法 当前使供体和受体同期发情的有效法是使用前列腺素或其类似物。但受体牛的给药时间要比供体提前一点。因为受体牛在前列腺素注射后72小时发情,供体牛在注入超排促性腺激素后隔一定时间才注射前列腺素,48小时后发情。这样两者才能同期化。
具体作法是: 用前列腺素或其类似物于母牛发情结束后3~15天(有活性黄体),在子宫颈内注射3 ~5毫克,或肌内注射20 ~30毫克。注入子宫颈内的药物有: 国产甲基前列腺素 (1~2毫克),前列腺素1α甲酯 (2~4毫克),以及13 -支氢前列腺素 (1~2毫克)。国外进口的高效前列腺素类似制剂肌内注射0.5毫克即可。
2. 阴道拴塞法 以清洁的泡沫塑料块,切成直径约10厘米、厚2厘米,拴上细线,线有足够长,一端放在阴门外10~15厘米 (便于处理结束时拉出)。所有药物参考用量: 甲孕酮150~200毫克,18 -甲基炔诺酮120~160毫克,甲基孕酮150~200毫升,氯地孕酮90~120毫克,氟孕酮180~240毫克,孕酮450~1000毫克。
塑料块不宜太小,防止滑脱; 也不宜太大,大了易引起母牛努责。吸上药液后,以长柄塞入母牛阴道内深部,子宫颈口处,放置两周左右 (14~16天取出)。当天全部牛只注射孕马血清促性腺激素1 000国际单位。用药后2 ~4天,母牛就表现同期发情。
3. 口服药物法 每日口服孕激素剂量为上述阴道药物量的1/5~1/8,平均投入精料中投喂,连续12~14天。最后一次口服的当天,肌内注射孕马血清促性腺激素1000~1200国际单位。
根据试验,上述方法的同期发情率为70%~90%。
同期发情处理效果如何,还受到药物种类、质量、投药方式,以及牛只的状况、季节等不同的影响,因此实行时应做好预试验,根据情况作适当处理。
三、供体母牛的超数排卵
牛是单胎动物,通常一个发情周期排一次卵。超数排卵是在母牛发情周期的某一时期,以外源性的促性腺激素处理母牛,而促使牛只卵巢多个卵泡同时发育,并且能够同时或准同时排出多个具有受精能力的卵子,这一技术称为超数排卵,简称 “超排”。促性腺激素常用孕马血清促性腺激素和促卵泡素,辅助激素常用促黄体素、人绒毛膜促性腺激素、促黄体释放激素。
(一)超排方法
1.PMSG+前列腺素F2α法
(1) 投药时间: 发情周期7~14天的任何一天。
(2) 剂量: 孕马血清促性腺激素2000国际单位。初配育成母牛2000国际单位或稍多,经产牛3000国际单位,老龄牛可用4000国际单位。
(3) 投药方法: 肌内或皮下一次注射,48小时后子宫颈注入前列腺素F2α2~3毫克或肌内注射前列腺素F2α15~25毫克 (如果用前列腺素的类似物则剂量为ICI79939 800微克或国产15-甲基前列腺素2微克)。
(4) 人工授精: 在注入前列腺素F2α48小时以后,一般都可发情,所以通常在这时采用定时输精。每隔8~12小时输精1次,每次输精量为常规的1倍。为了得到较多正常的胚胎,应使用活率高、密度大的精液,有必要进行3次输精。输精前最好进行直肠检查,触摸卵巢上卵泡的数量和大小以决定输精时间和次数。
2.FSH +前列腺素F2α法
(1) 投药时间: 在母牛发情周期7~14天的任何一天。
(2) 剂量: 促卵泡素总剂量40~50毫克,分4~5天肌内注射(国产品400~500大鼠单位,以第一次用量稍多,逐日降低剂量)。
(3) 投药方法: 每天上下午各投药1次 (肌内或皮下),间隔8~12小时,共计4~5天。每天的剂量一般是依次递减,有的国家是平均投药。前列腺素F2α的投药方法同PMSG+前列腺素F2α法相同。
3.FSH+前列腺素F2α+LH法
(1) 投药时间: 发情周期的7~14天的任何一天。
(2) 剂量: 促卵泡素总剂量50毫克。每天平均10毫克,上下午各肌内注射5毫克,每次各肌内注射促黄体素1毫克。投药48小时供体肌内注射前列腺素F2α,受体提早一天肌内注射前列腺素F2α。促卵泡素超排程序 (两个方法)
方法一 方法二
第1天午前 7毫克 5毫克
第1天午后 7毫克 5毫克
第2天午前 6毫克 5毫克
第2天午后 6毫克 5毫克
受体前列腺素F2α
第3天午前 5毫克 5毫克
供体前列腺素F2α
第3天午后 5毫克 5毫克
第4天午前 4毫克 5毫克
第4天午后 4毫克 5毫克
第5天午前 3毫克 5毫克
第5天午后 人工授精 人工授精
第6天午后 人工授精 人工授精
(3) 人工授精: 供体发情后即进行人工授精。母牛发情鉴定以接受爬跨为准,上午发现发情可进行第一次输精,也可以下午输精,视具体情况而定。
4. 供体牛同期超数排卵法 为了生产胚胎,提高工作效率,可视若干头供体同时超排采卵。
方法一: 供体牛皮下埋植孕激素,第7天注射孕马血清促性腺激素2000~3000国际单位,同时注射前列腺素类似物500毫克,第9天取出埋植物,发情后开始输精。
方法二: 供体牛3~4头为一组,于发情周期6~13天期间各注射前列腺素类似物ICI80996 500微克。发情后10天肌内注射孕马血清促性腺激素2000~3000国际单位。隔48小时再注射前列腺素类似物ICI80996 500微克。在此后,分别于56小时和72小时定时输精两次。回收胚胎的时间在第7~8天 (发情后) 回收移植效果好。
(二)影响母牛超排效果的因素
1. 母牛的个体差异 超排处理有1/3的母牛效果差。对这些牛可以改换超排药物,再行超排。
2. 母牛的年龄 青年牛的超排效果一般比经产牛好。可能是由于青年牛的机体对药物刺激有较高敏感性而造成的。
3. 牛品种的差异 据报道,超排处理在不同牛品种中反应有差异。如都以孕马血清促性腺激素作超排处理,则黑白花牛平均排卵5.3枚,西门塔尔牛12.2枚,而利木赞牛为16.4枚。另外还有季节的影响,如气温在27℃以上的高温对超排处理就有负面影响。日照长短也会影响处理效果。母牛的生理状态,如泌乳情况也是影响因素之一,如对处于泌乳高峰期的乳牛,则超排处理成功率大大降低。
四、胚胎的收集方法
牛的胚胎收集,目前一般都使用非手术法。
非手术法: 胚胎采集时间一般在母牛发情后7天,冲卵前,供体牛可不空腹,前肢站立位置稍高,必要时使用肚带,抬高前躯,为的是增加腹内正压,便于排出直肠内的粪便和空气。如是肉牛,应空腹24小时。
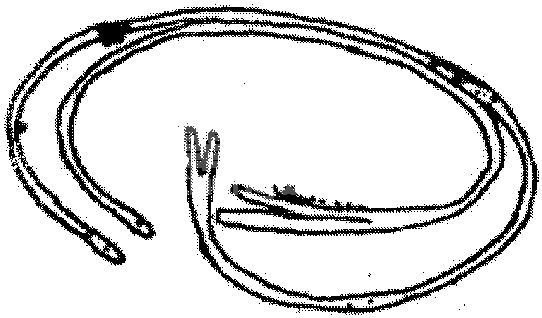
牛的非手术收集胚胎可利用二路式导管采卵器。关于采卵器,许多国家都有自己制造的非手术采卵器,其基本结构相同,不同之处主要是导管材料、长度、直径、气囊的位置和导管开口的多少等。有一、二、三路式采卵器。一般多用二路式,我国生产的二路式采卵器如附图1所示。
胚胎采集的操作要点如下:
(1) 供体牛保定以后,在第二或第三尾椎剪毛,药皂清洗,酒精棉球擦试。用2%普鲁卡因或2%利多卡因2~3毫升,进行硬膜外麻醉。如果不安定,肌内注射2%静松灵3~4毫升。
(2) 清洗会阴及外阴部,而后用70%酒精棉球擦净。
(3) 将尾巴拉向一侧: 为避免直肠过分努责,可将利多卡因滴在直肠黏膜上。
a
b
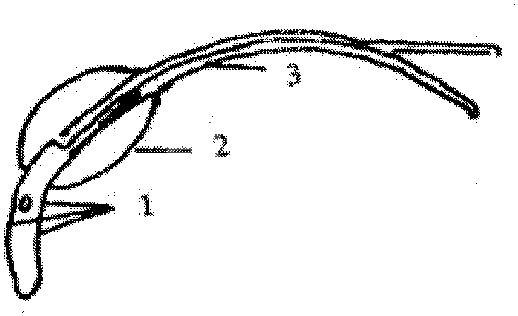
附图1 二路式采卵器
a.外观 b. 剖面观
1. 进出水孔2.气囊 3. 进出水通道
(4) 要努力避免在直肠中存有空气,这会降低触摸感受性及采卵率。必要时可用胃管将空气抽出。
(5) 检查卵巢的大小、子宫状况并估计黄体数。
(6) 对育成牛要先用子宫颈扩张棒扩张宫颈。
(7) 将不锈钢探针插入冲卵管,使其僵直。插前充气检查气囊并注入少许冲卵液,而后将它经子宫颈导入一侧子宫角内,其深度可使冲卵管达到子宫角前端 (大弯) 即可。用注射筒注入空气,使气囊膨胀,固定在子宫角内腔基部。初产牛充气12 ~15毫升,成年牛充气19~20毫升: 气囊过于膨胀易损坏子宫内膜,使其产生裂痕,冲卵液可渗透到黏膜的固有层内。气囊过小则不能固定冲卵管。一切妥当后,即可抽出探针。
(8) 冲卵管是三路式导管或二路式导管都可使用。前边将冲卵液通过中管注入子宫角,由内管导出,随进随出: 外管通入空气,使冲卵管前端的气囊膨大固定冲卵管 (气囊位置存在子宫角基部): 二路式冲卵管比较通用,冲卵液的注入和导出是同一通道,注入后停留片刻,然后导出。
进液的方式一般有两种: 一是用玻璃或塑料三通管连接冲卵管的进液管,使其分为注液管和出液管,注液管长约1米,上接一注液塑料管 (或注液)。注液时只要提高位置,冲卵液即可自然流入子宫。进液量由管夹或止血钳控制,夹住后,冲卵液即可导出,由连接的出液管流出直接导入量筒。二是用50毫升注射器抽取冲卵液,直接向进液管注入,使其注入子宫并由注射器回收。此法的优点是快速方便; 缺点是必须反复抽液和回收,如果进液快还可能损伤子宫内膜。
(9) 冲卵液及回收液的温度应是37℃。进液量每个子宫角约5000毫升,分若干次注入。原则上先少后多,前3次最重要,因为70%~80%的胚胎是由前3次冲出。
第一次进液20毫升左右。操作者通过直肠壁用拇指和食指捏住宫管连接部,使子宫充满卵液,其余手指捏住子宫角以逐出隐存子宫角内膜褶内的胚胎。第二、三次分别进液25~30毫升,以后逐次扩量至40 ~50毫升。轻轻按摩子宫角,如此即可将胚胎充分冲出。特别值得注意的是,冲卵开始时不得太急和莽撞,否则囊管结合部被挤开,胚胎由此流失。
(10) 冲完一侧子宫角迅速冲洗对侧角: 目前有两种转换方法:一是将气囊放气,拉出原管,另换冲卵管; 二是将冲卵管缓慢拉引到子宫体,使气囊位于子宫颈内口处,然后插入不锈钢丝至管顶端,放气后转向导入另一子宫角。
(11) 冲洗结束后,用注射器或导管往子宫内注入稀释后的青霉素或四环素。也可注30毫升0.05%的碘溶液。
(12) 冲洗后2~3天,子宫注入前列腺素F2a (或肌内注射),以使其尽快恢复发情。
(13) 冲卵管的清污和无菌至关重要,否则会造成细菌感染。冲卵管的冲洗程序如下:
使用后: 肥皂水冲洗→蒸馏水冲洗
使用前: 用酒精冲洗消毒→彻底用生理盐水冲洗
在正常情况下,冲卵液的回收率应在90%以上。当然回收卵液越充分,胚胎的收集率也越高。
当前,手术法冲卵多不采用,因为需要设备,操作时要进行麻醉,术后生殖器官容易粘连,缺点很多,不再叙述。
五、冲卵液和保存液的制作
冲卵液有很多种,即目前常用的是杜氏磷酸缓冲液 (PBS) 以及199培养液 (TCM199)。这些全合成的培养液不但用于冲洗收集胚胎,还可用于体外培养、冷冻保存和解冻胚胎等处理程序。
冲卵液和保存液的区别,就是前者可含可不含牛血清白蛋白(一般用犊牛血清代之),保存液则必须添加。冲卵液一般可添加血清1%~10%,保存液添加10%~20%。
杜氏磷酸盐缓冲液是比较理想而通用的冲卵液和保存液,室内和野外均可使用,配制比较方便。杜氏磷酸盐缓冲液和199培养液或其他培养液一般也有成品出售。
1. 杜氏磷酸缓冲液的配方 配制10升,需要: CaCl2·2H2O1.32克,MgSO4· 7H2O 1.21 克,NaCl 80克,KCL 2克,Na2HPO411.5克,KH2PO42克,葡萄糖 10克,链霉素硫酸盐0.5克,丙酮酸钠 0.36克,青霉素钠盐 100万单位
2. 配制方法
(1) 将NaCl、KCl、Na2HPO4、KH2PO4、葡萄糖、链霉素、丙酮酸钠、青霉素溶解在除去离子的8升蒸馏水中。
(2) CaCl2·2H2O、MgSO4·7H2O溶解在除去离子的2升蒸馏水中。
(3) 将2升加入8升水中并不停地搅拌均匀,否则会出现沉淀。
(4) 上述溶液用G6灭菌器(吸滤器) 过滤灭菌,在这程序中始终在无菌操作中进行。该溶液的氢离子浓度为pH值7.1~7.4。
(5) 冲卵用的杜氏磷酸盐缓冲液在使用前加1%的经过灭活的犊牛血清。保存液加20%。
3. 注意事项
(1) 牛羊血清对受精卵有毒性,这种致死因素没有耐热性,因此需要56℃条件下热处理30分钟将它破坏。
(2) 使用不含蛋白的溶液,受精卵容易在玻璃管壁上,因此需要加血清或血蛋白。
六、胚胎的检查和评定
回收到的冲洗液盛于玻璃器皿中,静置10 ~20分钟,待胚胎沉降到器皿底部,移去上层液就可以开始检卵,检查胚胎发育情况和数量多少。
在性周期第7日回收的牛的胚胎约100微米大小。因回收液中带有较多的黏液和血液,黏液常把卵裹在里面,不容易识别而被漏掉;血液中的红细胞藏住卵细胞,不容易看到,可用解剖针或加热拉长的小细管帮助查找。
(一)胚胎和检查
1. 用具
(1) 总倍率10~40倍的连续变倍和变更视野的解剖显微镜 (即实体显微镜)。
(2) 各种规格的有盖玻璃器皿或塑料皿,其深度为10~15毫米,直径为90~100毫米。为了检查方便,用小刀把皿外的底部刻画10~15毫米的线条。
(3) 小吸 (量) 管。可用结核菌苗注射器连接吸管或胶帽吸管。由于含有透明带的受精卵大小仅有0.15~0.20毫米,所以小吸管应加热拉细,使其直径为0.5~1毫米。玻璃小吸管需干燥灭菌。
2. 检查法 有两种检查法。
(1) 回收液镜检查: 这是在冲卵液少的时候,可把全液分成8~10份,放在检卵杯或玻璃皿中查找。
(2) 量筒法部分镜检: 有三种方法。
1) 把两角回收的大约1 000毫升冲卵液在量筒中静置约30分钟,使胚胎沉降。用小管虹吸的方法除掉上清液 (约需20分钟),把少量沉淀液分在若干培养皿内用实体显微镜检查。
2) 把回收液收到分液漏斗里,静置一段时间,从下部漏斗收集沉淀液进行镜检。
3) 把回收液放在100毫升的大试管里,静置后用吸管取底部沉淀液进行镜检。
这三种方法以量筒法较好,在有方格的培养皿中按纵横顺序进行检查,每个培养皿检查两次。在使用检卵杯检卵中,静置一段时间,检查胚胎集中的中央部分。检查时速度要快,不得超过30分钟,以防显微镜光源温度的影响。然后把找到的胚胎在200倍左右的生物显微镜下观察形态,进行鉴定。
(二)胚胎的评定
在超数排卵过程中,由于外源促性腺素的影响,使卵子通过输卵管的速度有所变化,所以回收的卵子中往往有未受精卵及退化卵,为了提供正常胚胎移植、所以须经过胚胎评定。常用的评定方法是形态学法。
1. 未受精卵 呈圆形,外周有一圈折光性强的透明带,中央为质地均匀、色暗的细胞质。透明带与卵黄膜之间的空隙很小,甚至看不到。
2. 受精卵的识别 有两个标准。一是第二极体的出现,二是卵周隙扩大。
(1) 发育正常的胚胎: 透明带发亮,卵周隙明显,分裂球大小均匀。一般来说,配种后5~6天采集的胚胎为桑葚期,7天后的为囊胚期,当然也有可能处于8~16个细胞的情况。
(2) 不正常的胚胎: 透明带变形,胚胎也变形; 有时透明带是圆的,但胚胎发暗; 卵裂球界限不清或细胞萎缩,卵周隙很大。
发育至不同阶段的早期胚胎以及异常胚胎的形态如附图2和附图3所示。
关于对早期胚胎从形态学上分类各有不同方法,加拿大穆特公司将配种后5~6天的正常发育卵分为A、B、C、D、E五级,A级最好。日本金川弘公司把受精后5~6天和胚胎同样分为A、B、C、D、E五类,A、B、C三类均或作为正常胚胎移植,D、E两类不能利用。国内将胚胎分为A、B、C三级,A级即优质胚,B级普通胚,C级不良胚。A级作冷冻保存用,B级作移植用,C级不能利用。
由于细胞形态和内在生命力并不一定有必然的相关性,所以不能把胚胎形态作为推测胚胎生命力的唯一标准,其他方法还有染色法、荧光法。在实际工作中可以根据胚胎的发育程度与发育的天数是否一致来判断。
如牛发情后的7~8天的胚胎,大多数是发育到桑葚期和囊胚初期。另一种方法是将胚胎进行培养,如胚胎继续发育,即说明胚胎是具有生命力的。
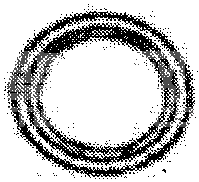
1细胞
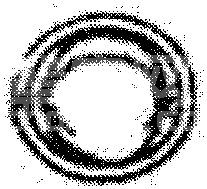
2细胞
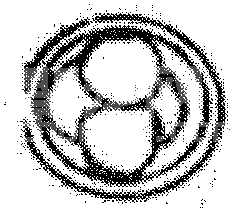
4细胞

8细胞
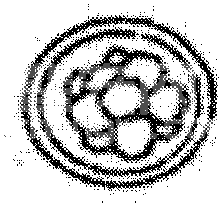
16细胞

桑葚胚

紧实桑葚胚
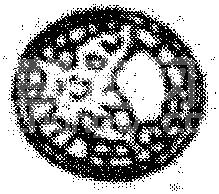
早期胚泡
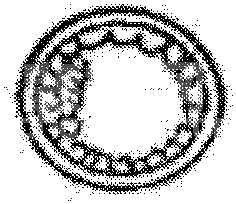
胚泡

扩张胚泡

脱出胚泡
附图2 发育至不同阶段的正常牛胚胎
七、胚胎的移植技术
移植技术分手术移植和非手术移植,目前多用非手术移植,此法在牧场及野外条件下都比较实用。非手术法移植如同人工授精,把胚胎注入子宫腔内。值得注意的是,经由子宫颈管进行胚胎移植,必须注意细菌污染,防止出血。胚胎移植时期是子宫的黄体期,子宫内部必须保存在无菌状态下,因此子宫颈管紧闭,与外界呈强的隔离状态。这是生理的最易感染期。在这样的生理状态下,通过子宫颈管而进行有胚胎移植,无菌操作则非常重要。

卵圆形透明带

卵裂球脱离
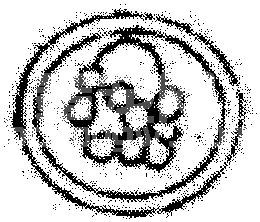
卵裂球不规则
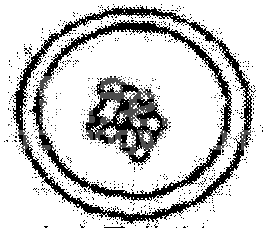
破碎桑葚胚
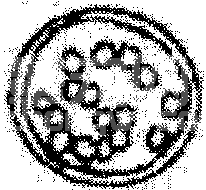
卵裂球分散
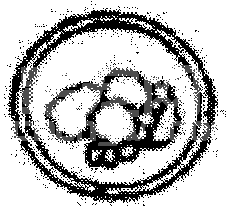
不规则细胞团
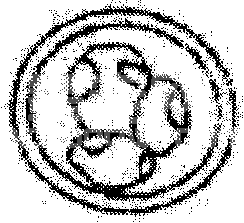
胞质中有空泡
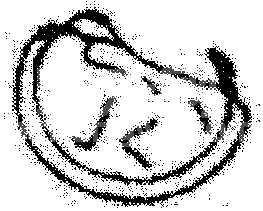
透明带破裂
附图3 形态异常胚胎
(一)药品、器材的准备
1. 麻醉剂 2%普鲁卡因或12%利多卡因及注射器和针头 (5毫升)。
2. 精液塑料细管 (0.25毫升或0.5毫升) 细管应是透明的,便于从外部观察受精卵。细管用氧化乙烯 (气体) 灭菌。
3. 输精用具 输精用卡苏精液注入器,或者使用带有塑料外鞘的卡苏式胚胎移植器 (外鞘可防止细菌等微生物污染)。
(二)移植程序
(1) 牛在保定栏或主柱上站立保定。为了便于直肠把握法的操作,用3~5毫升2%普鲁卡因或2%利多卡因进行尾椎硬膜外麻醉。
(2) 移植用的胚胎洗涤。把新鲜的冲卵液分在几个小皿,按顺序洗涤胚胎以除去附着黏液和血液等杂物。
(3) 细管内吸入胚胎。首先在细管内吸入保存液使其形成2~5厘米的液柱,接着使管内形成0.5厘米的空气层,然后再吸入含有胚胎的保存液,液柱为2.5厘米,再形成一空气层,再吸入少量保存液。在吸入时,吸管可连接1毫升注射器,操作比较方便。吸入时要使用实体显微镜,吸入后还要隔细管壁检查,以确定它是否在保存液中。
(4) 移植器的安排。把吸入胚胎的细管安装在精液注入器上,并套上灭菌的外鞘。
(5) 受体消毒。用温水或肥皂水清洗外阴部,以干布或卫生纸擦拭,然后再用消毒液洗涤,最后用70%酒精棉球擦之。
(6) 插入移植器。把套上外鞘的移植器插入阴道内,并推进子宫颈口,使移植器冲破外鞘的前端直接伸进子宫颈内。育成牛子宫颈管细,移植器插入前可先用子宫颈扩张棒扩张。
(7) 移植器进入黄体一侧的子宫角内。这时用伸进直肠的手把握子宫角,使其达到子宫角的游离部稍前的位置 (大弯),随即将胚胎推出。移植不超过10分钟,动作轻、快、稳,移植后应清洗细管和移植器前端,镜检胚胎是否被漏掉。牛胚胎一般在排卵一侧的子宫角着床,很少向对侧子宫角移动,因此在排卵侧受胎率较高。但非排卵角有时也能受胎,所以给肉牛每侧各移一个也能获得双胎。
(三)移植适宜时期
移植胚胎给受体,一般是受体在发情后的第7天。如果只根据天数,成功率不会太高,关键是受体牛黄体发育最适宜的时候移植,才能获得理想的效果。在移植前,要对受体牛仔细进行检查。如果黄体发育到所要求的程度,即使与发情后的天数不吻合也可以移植; 反之,就不能移植。胚胎移植受体后,须加强护理,尤其是手术后。移植后不要频繁地进行直肠检查,防止流产。牛胚胎早期的死亡率较高,并且主要发生在27天以前。移植后2个月,若不见受体发情,可以直肠检查1次,初步确诊是否妊娠。
(四)胚胎冷冻保存
牛的胚胎一般进行短期保存和冷冻保存。从冲卵一直到移植,如果使用鲜胚,只要在1小时或几小时内完成,这段时间保存在室温(18~25℃或37℃) 环境里受胎率没有差别。鲜胚的移植受胎率现在可以达到50%~70%,而冻胚在一般情况下,可以达到45% ~50%,但一般低于这个比率。冷冻保存是今后的方向,如同冻精,可长期保存,用价值很大。胚胎冷冻以7~8日胚龄的受精卵为好。
目前对于牛胚胎冷冻保存试验虽有多种经过改进的方法,但基本程序如下: 添加低温保护剂,进行平衡; 将胚胎装进细管里,放进降温器里,诱发结晶; 慢速降温; 投入液氮 (-196℃) 中保存; 升温解冻; 稀释脱除胚胎里冷冻保存剂。
现行胚胎冷冻法主要有以下三种:
1. H.Niemann实验室采用冷冻法 其冷冻程序是: ①在室温下,将胚胎直接放进含1.4摩尔/升甘油的杜氏磷酸盐缓冲液中,平衡20分钟。②把胚胎放进0.25毫升细管里,两头再吸进冷冻液,三段液之间以空气隔开。③把装有胚胎的细管放在1 ~7℃的乙醇里。④用超低温夹器夹细管以诱发结晶,然后平衡5分钟。⑤以0.3℃/分钟速度再继续降到-28℃。⑥以0.1℃/分钟速度降至-35℃。⑦投入液氮 (-196℃)。⑧30℃温水浴中解冻。⑨分两步用蔗糖液脱除冷冻保护剂。
7日龄的牛胚 (桑葚胚和囊胚) 比8日龄的膨胀囊胚更适合快速冷冻,膨胀囊胚用慢速冷冻存活率较高; 血液孕酮浓度为2~5纳克/毫升的受体母牛,胚胎移植的妊娠率较高,而高于或低于此浓度的受体妊娠率较低。
2. 一步冷冻解冻法 一步冷冻解冻法是由慢速冷冻法改进来的,省去了冷冻后脱除冷冻保护剂和形态学评定操作,其要点是细管里的冷冻液和稀释液是分开的。下面介绍新疆畜牧科学院畜牧所郭志勤等的试验 (一步细管 “冷冻保存技术”)。以20%犊牛血清的杜氏磷酸盐缓冲液,配制成为10%甘油防冻保护液。以12.5%蔗糖液脱甘油。需要冷冻的胚胎直接移入10%甘油中,装管置冷冻仪、植冰,然后以0.5℃/分钟降至-30℃,平衡后投入液氮。解冻为25℃或37℃水浴,经F-10培养液培养。解冻胚发育率为65.0%和77.4%。冻胚解冻后脱甘油是在细管内进行的,现场操作,现场移植。一支细管装1枚胚胎,1988年受体牛为杂种母牛,用该法输冻胚的妊娠率为41.38%。
一步细管法的特点是从解冻到移植的全过程可以现场进行,操作简单,易于掌握,便于推广,但仍需进一步研究改进提高妊娠率。
3. 玻璃化法 此法是最新的快速冷冻方法,它不要冷冻器。这种方法是按物理学原理将高浓度的低温保护剂凝固,而不形成冰晶,其结构仍保持正常分子状态,在液体中则成离子分布,因此称作玻璃化法。目前用较简单的玻璃化液的组成是25%的甘油、25%丙二醇,下面介绍一个日本的试验报道。
试验步骤: ①配制玻璃化液,是以添加20%新生犊牛血清的杜氏磷酸盐缓冲液为基本液配制10%甘油和20%丙二醇的混合液为第一液。②以25%甘油和25%丙二醇的混合液为第二液。③配制含有1摩尔/升蔗糖的杜氏磷酸盐缓冲液作为玻璃化液的稀释液。④将胚胎浸渍在第一液中平衡10分钟。⑤将平衡后的胚胎移入第二液中。⑥装管。一支0.25毫升塑料细管装1枚胚胎。⑦含有胚胎的第一液和第二液预先冷却并保持4℃。⑧将装胚胎的细管按照Taka -hansh和Kanagawa (1985) 的方法,放置浮在液氮上的苯己烯泡沫板上。⑨当蔗糖结冰时投入液氮中。从第一液移到第二液以及到液氮中静置的时间为23 ~76秒。
解冻: 将细管放在20℃的恒温槽内,约浸渍10分钟 (至蔗糖层完全融解) 解冻。解冻后立即将细管内溶液全部取出,混合放置在塑料小皿内,室温下静置5分钟后移到杜氏磷酸盐缓冲液中,胚胎经杜氏磷酸盐缓冲液洗净后,置于倒置显微镜下,观察其形态,仅将判断为正常的胚胎供移植。
试验结果: 解冻后的桑葚胚70%形态正常,移植给受体母牛,受胎率达57.1%,而囊胚在解冻后无一成活。
八、胚胎生物工程技术的新进展
(一)胚胎分割
胚胎分割是一项正在发展的技术。分割时,在显微镜下将早期胚胎 (2~8细胞期) 切割为两部分或多个部分,从而生产同卵多头犊牛,这在牛的遗传育种方面有很大价值。在这方面,我国也已试验成功。1986年西北农业大学主持的奶牛胚胎切割移植黄牛成功率40%。
目前,实行这一技术还有一些限制,这包括: 尚不能对受精卵发育至更广阔的 (如超过16细胞以上) 胚龄胚胎作分割移植; 也不能对2~8细胞期重复切割,切割多于4部分的胚胎尚不能正常发育,分割后的胚胎冷冻和解冻时存活率大大降低。
(二)体外受精
体外受精是一项使精子与卵子在母体外实现受精而结合成为有生命合子的一种技术。1981年美国已有成功的先例,生下世界上第一头体外受精犊牛。目前,体外受精已在多种家畜和人类中研究成功。
体外受精具有巨大的潜在价值。在自然状态下,母牛一个情期仅排卵一枚,每年产犊的母牛一生也不过有效利用10多个卵子。可是卵巢中却有数十万个卵母细胞存在。就公牛而言,据测算,一次射精所含有的精子数量可以满足3.6万个卵母细胞受精,而制成细管冷冻精液时,一般仅能生产600头份 (支) 的数量。可见,无论公、母牛,潜力都是巨大的。同时挖潜公、母牛繁殖潜力的技术方法之一就是体外受精技术。
(三)性别控制
哺乳动物的性别是由染色体决定的。而母性总是带有X染色体,只产生一种带X的配子; 而雄性的性染色体为异型染色体,可产生两种配子,即X和Y两种精子,X生成雌性,而Y生成雄性,所以决定性差异的原因在于这两种精子的存在。
牛是哺乳动物,也受上述规律的支配。长期以来,人们一直寻求一种简便而可靠的方法,以便使包括牛在内的家畜性别,按照人的愿望而产生。
性别控制在家畜生产中有很大的意义。例如某些限性经济性状在一种性别家畜中体现 (如产奶),还有经济性状、生产力虽然在两种性别个体上都表现,但某一性别的生产力却显著地高于另一性别(如羊的产毛量,肉用公牛的产肉量、生长强度等)。为适应生产发展的需要,人们对性别控制的追求热情经久不衰。
研究的焦点集中在对公畜的X精子与Y精子的分离方面。
X精子与Y精子的区别。哺乳动物细胞分裂中期,可以看出性染色体对中的X染色体明显大于Y染色体。牛的X染色体比Y染色体面积要大1倍多,这种差异也会影响精子的运动与静置的沉降速度。
研究结果新近又发现,真正决定性别的物质存在于Y染色体的长臂一端叫作F小体中。凡能检测到含有F小体的精子均决定雄性的Y精子,否则就是X精子。
